Date: Aug 2020
Um ein reflektierteres Modell für die Reaktion von Tumorzellen in-vivo auf Testmittel zu liefern, muss die Gewebephysiologie, in der der Tumor wächst und sich vermehrt, in-vitro rekapituliert werden. This process has been accomplished using Predictive Oncology® organ-specific three-dimensional (3D) matrices that support long-term culture of carcinoma cells. Labcorp and Predictive Oncology® have worked together to develop tumor-specific 3D models, based on Predictive Oncology® proprietary 3D cell culture platform for preclinical testing and research studies in the biopharmaceutical industry. Dieses Tech-Spotlight erläutert die Eigenschaften des rekonstruierten Knochenmodells (r-Knochen).
Das Wachstum von Tumorzellen im Knochenmark ist ein häufiges Phänomen bei hämatologischen Malignitäten. Daher wurden humane Myelomzelllinien RPMI 8226, NCI-H929 und U266B1 in Machbarkeitsstudien verwendet. Wie in Abbildung 1 dargestellt, wurden U266B1 humane Myelomzellen ausschließlich im Wachstumsmedium (2D) oder in r-Knochen-Matrix für 4 Tage kultiviert. Während die 2D-Kultur schnell überwachsen wird und die Zellen eine Morphologie beibehalten, die durch eine einzelne Zellsuspension gekennzeichnet ist, unterstützt die r-Knochen-3D-Kultur die Entwicklung von Zellaggregaten, die sich stärker zu größeren Clustern vermehren und die Tumormorphologie besser darstellen. Diese Kulturen können mit nur geringfügigen Eingriffen des Forschers über lange Zeiträume aufrechterhalten werden.
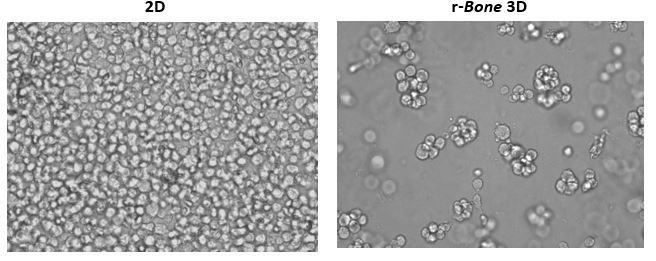
Abbildung 1: 2D gegenüber rekonstruierter Knochen-3D-Kultur von U266B1 menschlichen Myelomzellen
Figure 2 shows cryo-electron microscopic images of r-Bone culture and ex vivo bone marrow seeded with metastatic breast cancer cells. Die räumliche und physikalische Architektur des Knochenmarkstromas bleibt in der extrazellulären r-Knochen-Matrix (ECM) erhalten. Die r-Knochen-ECM ermöglicht die Co-Kultur von Tumorzellen mit mesenchymalen Stammzellen, Fibroblasten, lymphoiden, myeloiden und CAR-T-Zellen.
Zellen können nach Exposition des Testmittels aus der Matrix isoliert und durch eine geeignete nachgeschaltete Anwendung wie Durchflusszytometrie, RNASeq oder In-situ-Bildgebung analysiert werden. Zytotoxizitätsassays wie CellTiter-Glo® können in einem hohen Durchsatzformat durchgeführt werden, wobei sowohl 96- als auch 384-Well-Assay-Formate erfolgreich entwickelt werden. Die Plattform ist mit allen getesteten Wirkstoffklassen kompatibel, einschließlich Biologika und kleinen Molekülen.
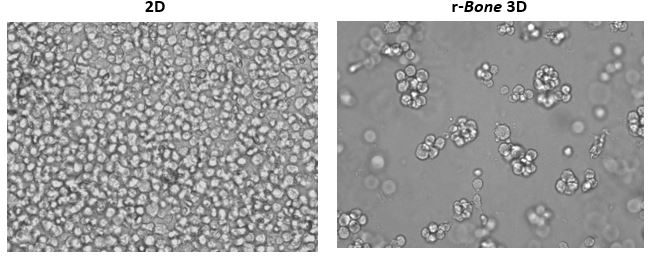
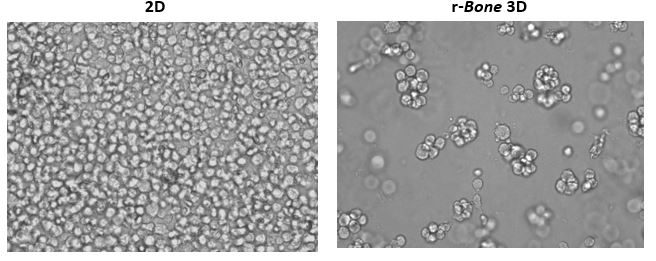

Abbildung 2: Die extrazelluläre Matrixarchitektur von r-Knochen ist von Ex-vivo-Gewebe nicht zu unterscheiden
Abbildung 3: Bortezomib ist ein Standardmittel zur Behandlung des multiplen Myeloms2. Nach 4-tägiger Kultur von NCI-H929-, RPMI8226- und U266B1-Zellen in r-Knochen wurde Bortezomib zugegeben und die Zellen wurden für weitere 4 Tage in die Kultur zurückgegeben. (A) CellTiter-Glo®-Reagenz wurde zugegeben und die Lumineszenz wurde unter Verwendung eines Cytation 3-Plattenlesegeräts zur Bildgebung (Biotek Instruments) quantifiziert. Die nichtlineare Kurvenanpassungsanalyse mit vier Parametern wurde gegen die mit einem Träger behandelten Wells normalisiert (n = 3 Wells pro Konzentration). (B) Repräsentative Bilder von U266B1-Zellen in einer r-Knochen-Kultur, die mit einem Träger (0,5 % DMSO) oder 20 nM Bortezomib behandelt wurde. Die roten Pfeile zeigen tote oder sterbende Zellen in den Zellclustern nach 72-stündiger Exposition an.
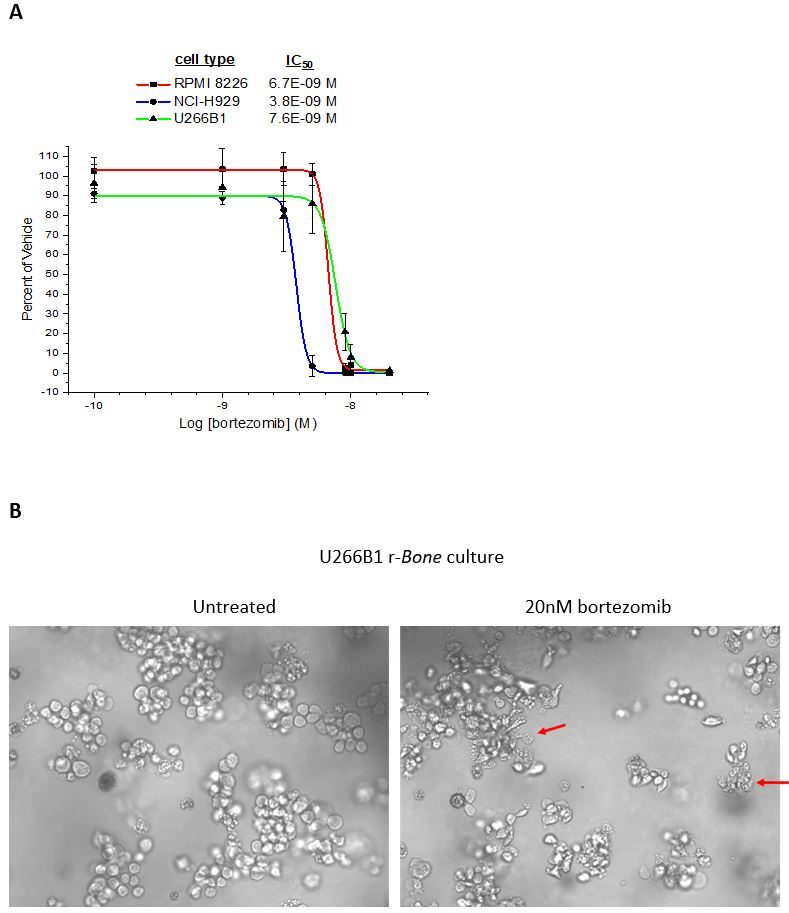
Abbildung 3: Bortezomib-Hemmung der Myelomzellproliferation in r-Knochen-Kultur
Der r-Knochen-Assay ist eine potenzielle Plattform für die Untersuchung multipler hämatologischer Malignome in-vitro sowie für die Untersuchung von soliden Tumormetastasen wie Brust- und Prostatakarzinomen in der Knochenmatrix.
Predictive Oncology® has provided customized tumor-specific 3D cell culture models since 2014 and has been actively developing numerous organ-specific matrices to broaden the preclinical tumor offerings since we've been working together.
Rekonstruierte Brust der Maus (r-mBrust) und menschliche Brust (r-Brust), Lunge (r-Lunge) und Prostata (r-Prostata) werden derzeit charakterisiert und entwickelt. Diese Modelle werden neue frühe Möglichkeiten darstellen, Testmittel auf einer Plattform zu screenen, die In-vivo-Gewebemikroumgebungen genauer nachahmt, ohne im Vorfeld in Tierstudien zu investieren. Das Potenzial, gezielte chemische Bibliotheken in einem 3D-Assay mit hohem Durchsatz zu screenen, sollte bei frühen Bemühungen im Entdeckungsprozess berücksichtigt werden.
For more information on how these 3D model assays can be applied to your preclinical oncology and immuno-oncology research, contact our scientists below.
Verweise
1. Edmondson R, Broglie JJ, Adcock AF, Yang L. Three-dimensional cell culture systems and their applications in drug discovery and cell-based biosensors. Assay Drug Dev Technol. 2014;12(4):207-218.
Unterhalten wir uns
Kontakt