Autor: Erin Trachet, PhD | Direktorin, Wissenschaftliche Entwicklung
Date: September 2019
Brustkrebs ist nach wie vor eine der am weitesten verbreiteten und lebensbedrohlichsten Krankheiten bei Frauen weltweit. Nach Angaben der American Cancer Society gab es unter den US-amerikanischen Frauen 2017 ungefähr 253.000 neue Fälle von invasivem Brustkrebs, die zu 41.000 Todesfällen führten.[1] Etwa 6–10 % der neuen Brustkrebsfälle (15,000–25,000) werden als metastasierend (Stadium IV) diagnostiziert. Man geht jedoch davon aus, dass 20–30 % aller Brustkrebs-Fälle im Laufe der Zeit metastatisch werden.[1]
Tiermodelle können sehr leistungsfähige Instrumente zur Analyse der Entwicklung und des Fortschreitens von Krebs sein. Ein Beispiel dafür ist das Modell des transgenen mittleren T-Onkoproteins (PyMT) des Polyoms. Die Expression der PyMT ist durch den MMTV-Promoter/Verstärker auf die Brustdrüsen beschränkt und führt zu Mäusen, die vier verschiedene Stadien der Tumorprogression vom prämalignen zum malignen Stadium durchlaufen. Diese Stadien sind mit dem menschlichen Brustkrebs vergleichbar. Zusätzlich zu den morphologischen Ähnlichkeiten mit menschlichem Brustkrebs ist die Expression von Biomarkern in MMTV-PyMT-induzierten Tumoren auch konsistent mit denjenigen, die mit einem schlechten Ergebnis beim Menschen assoziiert sind. Dazu gehören der Verlust von Östrogen- und Progesteronrezeptoren und die anhaltende Expression von ErbB2/Neu (Her2) und CyclinD1 in MMTV-PyMT-Tumoren auf dem Weg zum malignen Stadium.[2]
Given the desperate need, and the uniqueness of the MMTV-PyMT model, Labcorp has developed and optimized a transplantable version of this model that’s derived from transgenic host mice (FVB/N-Tg(MMTV-PyVT)634Mul/J).
Primäres Brustfettpolster-Tumorwachstum
Die orthotopische Primärtumor-Wachstumskinetik für das transplantierbare MMTV-PyMT (PyMT)-Modell ist in Abbildung 1 dargestellt. Die mediane Verdopplungszeit beträgt ~8 Tage mit einer stetigen Zunahme des Tumorvolumens und keinem offensichtlichen tumorbedingten Körpergewichtsverlust. Als die Tiere aufgrund des Primärtumorwachstums eingeschläfert wurden, wurden Lungenknötchen festgestellt. Die Wachstumsrate erlaubt ein vierwöchiges therapeutisches Fenster zur Evaluierung von Anti-Tumor-Reaktionen.
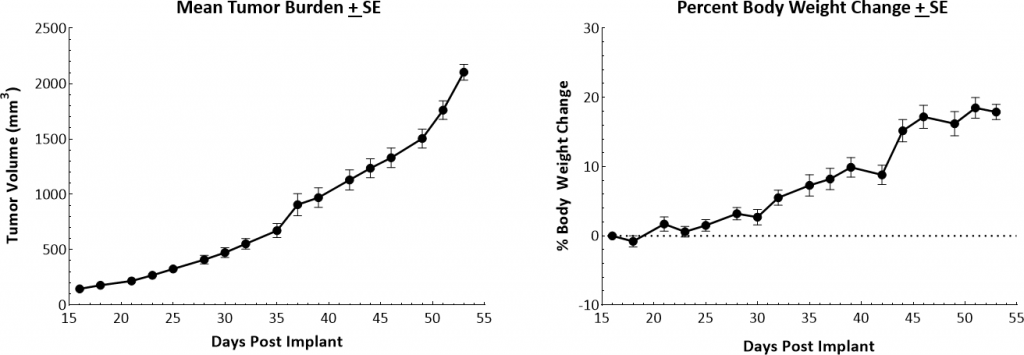
Abb. 1: Wachstumskinetik und Körpergewichtsveränderungen von MMTV-PyMT-Tumoren bei weiblichen FVB/NJ-Mäusen.
Immunprofil des PyMT-Tumors
The baseline tumor immune composition was analyzed by flow cytometry and is shown in Figure 2. The lymphoid population has an equal distribution of CD8+ and CD4+ T cells. Während NK-Zellen eine beträchtliche Präsenz aufweisen, sind B-Zellen und NKT-Zellen nur minimal vertreten. Die Tumoren haben eine große myeloische Population, die überwiegend durch G-MDSCs und M1-TAMs repräsentiert wird. Die Infiltration von CD8+ T-Zellen und NK-Zellen unterstützt die Theorie, dass das PyMT-Modell auf immunmodulierende Agenzien reagieren könnte. Es gibt jedoch auch beträchtliche myeloische Suppressorzellen innerhalb der Tumor-Mikroumgebung. Daher haben wir die Reaktion auf immunmodulierende Wirkstoffe getestet (siehe Abbildung 3), um festzustellen, ob das PyMT-Modell eher einem immunsuppressiven „kalten“ Tumor oder einem immunreaktiven „warmen“ Tumor entspricht.
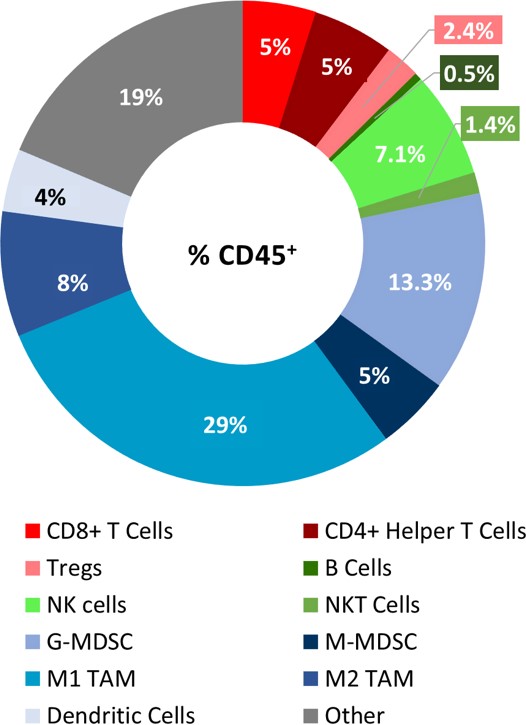
Abbildung 2: Immunprofil von PyMT-Tumor-Infiltraten
Reaktion auf Checkpoint-Blockade und Behandlungen mit fokussierter Strahlung
Zur Evaluierung der Anti-Tumor-Antwort auf immunmodulatorische Wirkstoffe wurden Mäuse, die orthotope PyMT-Tumore trugen, mit Checkpoint-Blockade-Antikörpern (anti-mPD-1, anti-mPD-L1 und anti-mCTLA-4) und Fokalbestrahlung behandelt. Die Behandlung mit Einzelwirkstoff-Kontrollpunktinhibitoren zeigte ein mildes Ansprechen, das zu Verzögerungen des Tumorwachstums von 3–6 Tagen, aber zu keinen Tumorregressionen führte (Abbildung 3). Orthotope PyMT-Tumoren reagieren nur geringfügig auf die Behandlung mit Checkpoint-Inhibitoren, so dass eine klare Chance besteht, dass eine Kombinationstherapie zusätzlichen Nutzen zeigen könnte. Darüber hinaus legen diese Daten nahe, dass das Modell eher in ein „kaltes“ Tumorprofil passt.
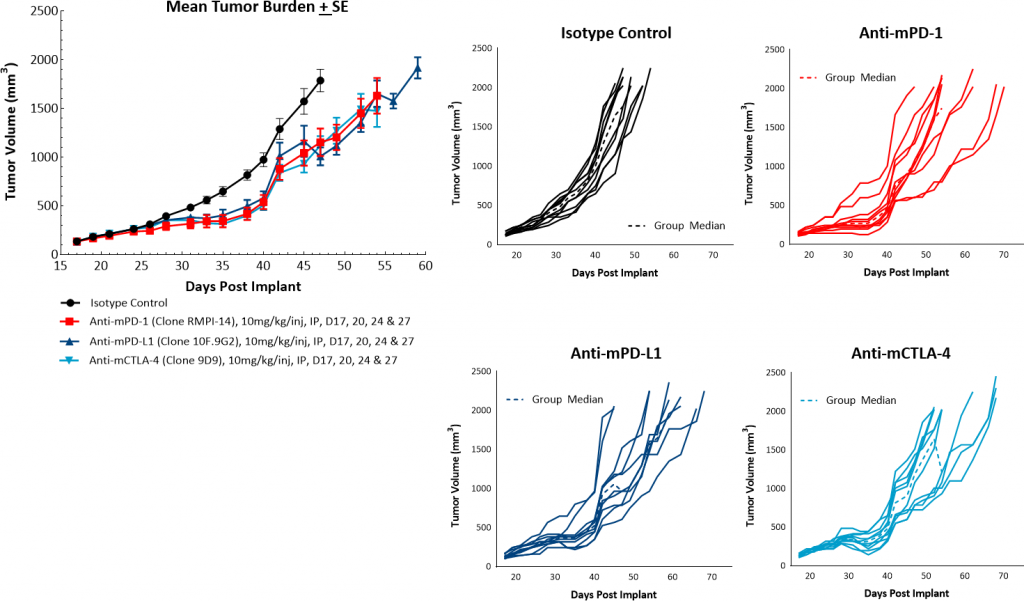
Abb. 3: PyMT-Reaktion auf Checkpoint-Inhibitoren.
Zusätzlich zur Checkpoint-Blockade wird die fokale Bestrahlung auch als nützlicher Behandlungsansatz zur Modifizierung einer immunsuppressiven Tumor-Mikroumgebung angesehen. Darüber hinaus ist die Strahlenbehandlung für viele Brustkrebspatientinnen eine gängige Therapie. Labcorp utilizes the Small Animal Radiation Research Platform (SARRP; Xstrahl) to provide focal radiation therapy to mice in a manner consistent with radiation treatment in patients. In diesem Modell testeten wir einzelne, fokale Strahlendosen von 5, 10 oder 20 Gy und stellten fest, dass sie gut verträglich und hochwirksam sind. Sowohl die 20- als auch die 10-Gy-Dosierungen führten zu starken Anti-Tumor-Reaktionen mit einer Inzidenz von 100 % bzw. 38 % der vollständigen Responder (Abbildung 4). Auf Grundlage dieser Daten würde eine Einzeldosis von 5 Gy-Fokalstrahlung für Kombinationsstudien empfohlen.
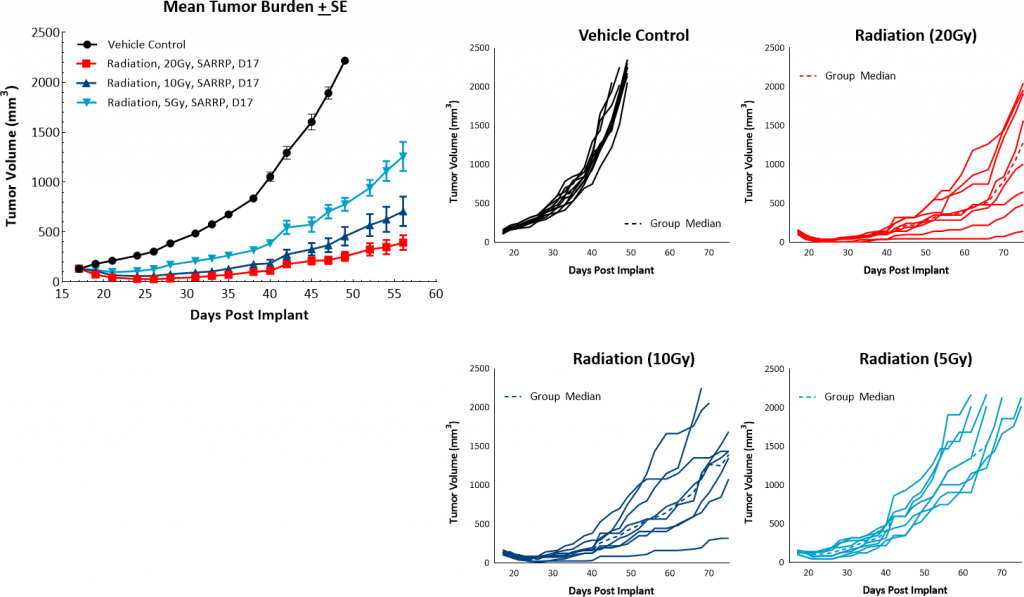
Abb. 4: PyMT-Reaktion auf fokale Strahlung.
Übersicht
Transplantierbares PyMT ist ein sehr nützliches Modell zur Evaluierung von Wirkstoffen, die auf das Mammakarzinom abzielen. Dieses Modell bietet der Forschungsgemeinschaft die Möglichkeit, ein Modell zu verwenden, das viele Aspekte und Komplexitäten der klinischen Erkrankung widerspiegelt. Viele klinische Ansätze bei Brustkrebs schließen jetzt Immuntherapien und/oder Strahlentherapie als Teil der laufenden klinischen Studien ein. Die Daten, die wir hier skizzieren, legen nahe, dass das PyMT-Modell für Kombinationsstudien mit entweder Checkpoint-Inhibitoren oder niedrig dosierter fokaler Strahlung geeignet ist. Contact Labcorp to learn more about our transplantable PyMT model or other breast cancer models that we offer.
Verweise
Unterhalten wir uns
Kontakt