Author: Erin Trachet, BS | Associate Director, Scientific Development
Date: March 2021
Lungenkrebs breitet sich rasch auf andere Körperteile aus. Einer der gefährlichsten Bereiche, in die er streuen kann, ist das Gehirn. Dies senkt die Lebenserwartung erheblich. Leider kommen diese Metastasen häufig vor. Bis zu 7 % der Menschen haben bereits Krebszellen im Gehirn, wenn bei ihnen erstmals nicht-kleinzelliger Lungenkrebs (NSCLC) diagnostiziert wird, und 20 % bis 40 % der Menschen mit NSCLC werden diese Komplikation während des Fortschreitens der Krankheit entwickeln. Hirnmetastasen treten im 4. Stadium von Lungenkrebs auf. Lungenkrebs im 4. Stadium hat eine schlechte Prognose, wobei die Lebenserwartung normalerweise unter einem Jahr liegt1.
Derzeit gibt es keine gezielten Therapien spezifisch für Hirnmetastasen, und die Blut-Hirn-Schranke kann ein physiologisches Hindernis für viele Zytostatika und auf Antikörpern basierende Therapien darstellen. Chirurgische Tumorresektion und/oder Strahlentherapie sind die am häufigsten verwendeten Behandlungsformen, aber die allgemeine Verlängerung der Überlebenszeit ist geringfügig (~4 bis 6 Monate) und die Lebensqualität nach der Behandlung kann sehr gering sein2. Es ist offensichtlich, dass für diese verheerende Krankheit wirksamere Behandlungen benötigt werden. Die Fachliteratur präsentiert nur sehr wenige präklinische Onkologiemodelle, die die Beurteilung metastatischer Gehirnerkrankungen bei Vorhandensein eines Primärtumors erleichtern. In recognition of this need, Preclinical Oncology (PCO) has developed two xenograft models to not only address metastatic brain disease via a direct intra-cranial implant, but also couples this with a subcutaneous “primary” tumor to effectively allow the evaluation of the response to treatment at both locations.
Darüber hinaus ist es wichtig, die Pharmakokinetik und/oder Pharmakodynamik (PK/PD) gezielter Therapien an beiden Implantatstellen gleichzeitig beurteilen zu können. Die Behandlung mit gezielten Therapien kann bedeutend unterschiedliche Penetrations- und Absorptionsraten aufweisen, was die PK/PD-Beurteilung in beiden Geweben verändert. Angesichts der einzigartigen Umgebung im Gehirn und des Hindernisses, das die Blut-Hirn-Schranke für einen Vergleich zwischen den beiden Stellen darstellt, kann dies ein leistungsstarkes Instrument sein, um die Auswirkungen der Behandlung auf bestehende metastatische Erkrankungen und Primärtumore zu bewerten.
PCO hat den Induktionsparameter für doppelte Krankheiten für zwei humane nicht-kleinzellige Lungenkarzinomzelllinien optimiert; NCI-H1975-luc and PC-9-luc. Beide Zelllinien wurden mit Luciferase transfiziert, um eine Biolumineszenz-Bildgebung (BLI) zu ermöglichen und so das Fortschreiten der Krankheit für die intrakraniell implantierten Zellen zu überwachen. Die subkutanen „primären“ Tumore sind abgeschirmt, um überlappende Signale zu verhindern. In allen Studien mit Tieren wurden die gesamte Tierpflege und -nutzung gemäß den Tierschutzbestimmungen in einer AAALAC-akkreditierten Einrichtung mit Überprüfung und Genehmigung des IACUC-Protokolls durchgeführt.
NCI-H1975-Luc
NCI-H1975 wurde aus einer Nichtraucherin erstellt. Diese Zelllinie ist aufgrund ihres EGFR-L858R/T790M-Mutationsstatus für die Forschungsgemeinschaft von Interesse. Die mit T790M erworbene Mutation wird bei 50 bis 60 % der NSCLC-Patienten gefunden, die gegen genehmigte EGFR-Inhibitoren resistent werden. Daher eignet sich dieses Modell zur Bewertung von EGFR-Inhibitoren der nächsten Generation, wie Verbindungen, die sich unabhängig von den aufgetretenen Mutationsänderungen an EGFR binden, oder Verbindungen, die sich irreversibel binden. Das EGFR-Expressionsprofil von NCI-H1975-luc hat es zu einem interessanten Modell für die Doppelimplantationsmethode gemacht, da es die Beurteilung der Penetration der Blut-Hirn-Schranke eines auf EGFR gerichteten kleinen Moleküls ermöglicht. Diese Bewertung kann auf verschiedene Arten erfolgen. Die traditionelle Wirksamkeit basiert auf der BLI-Überwachung der metastasierten Gehirnerkrankung in Verbindung mit Messschiebermessungen der subkutanen Tumore und/oder der pharmakodynamischen und pharmakokinetischen Analyse der metastatischen Läsion im Vergleich zu den Primärtumoren. Ziel ist es, festzustellen, ob die Wirkstoffkonzentrationen sich unterscheiden. In beiden Szenarien kann die metastatische Gehirnerkrankungsreaktion dann mit der „primären“ subkutanen Tumorreaktion verglichen werden.
In Übereinstimmung mit dem historischen Tumorwachstum für dieses Modell beträgt die Verdopplungszeit des subkutanen Tumorvolumens etwa 7 Tage und erreicht typischerweise die Bewertungsgröße (~900 mm3) in ungefähr 25 Tagen nach der Implantation (Abbildung 2). Wie erwartet ist das Modell bei intrakranialer Implantation genauso zuverlässig, mit einer per BLI berechneten Verdopplungszeit des Tumorvolumens von 1,6 Tagen (Abbildung 1 und Bild 1).
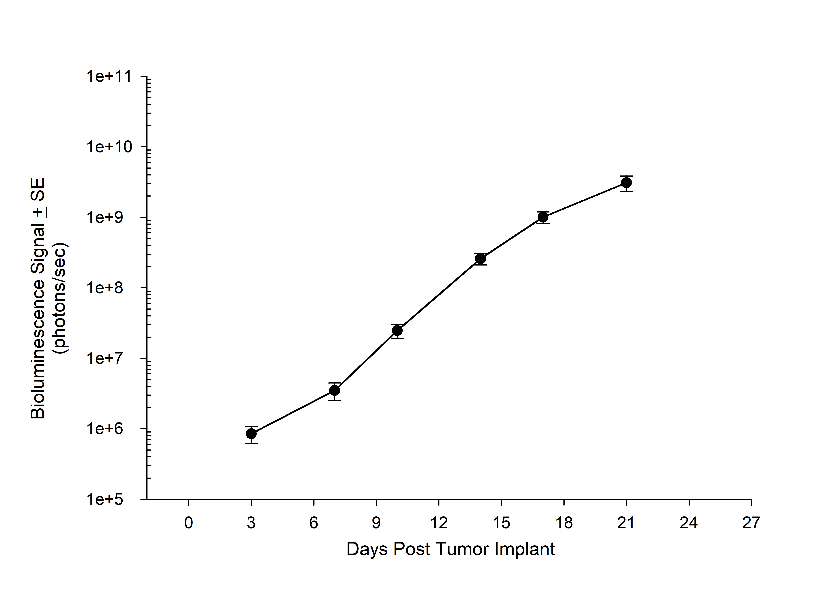
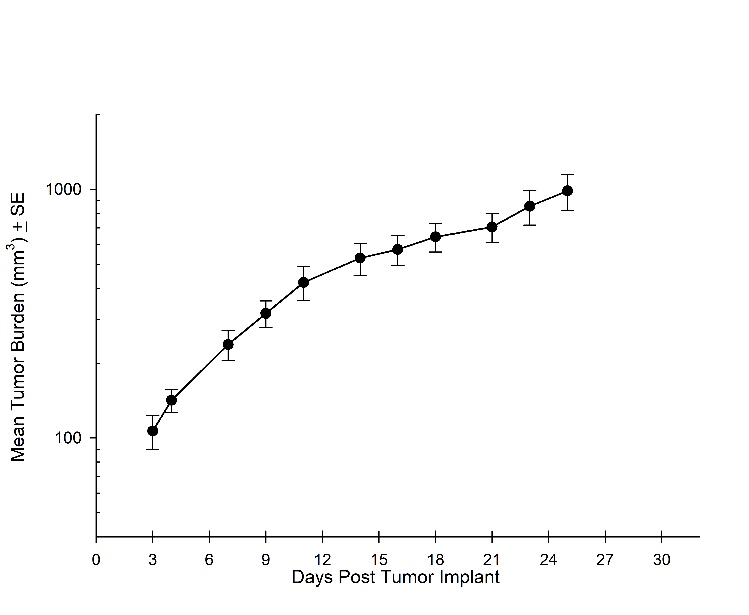
Abbildung 1A: NCI-H1975-Luc mittleres BLI-Signal für das Fortschreiten der metastasierenden Erkrankung
Abbildung 2A: NCI-H1975-Luc mittleres Wachstum des Primärtumors (SC)
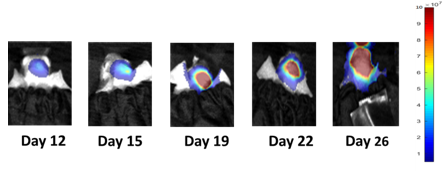
Bild 1: NCI-H1975-Luc repräsentative Bilder des Fortschreitens der metastasierten Gehirnerkrankung
PC-9-Luc
PC-9-Luc wurde 1989 aus einem männlichen Lungenadenokarzinom-Patienten isoliert. Es wurde dargelegt, dass PC-9-Luc sehr empfindlich gegenüber Gefitinib und anderen EGFR-Tyrosinkinasehemmstoffen ist. Es wurde jedoch gezeigt, dass eine längere Exposition von PC-9-Luc-Zellen gegenüber EGFR-Inhibitoren zum Erwerb der T790M-Mutation und einer resistenten Zelllinie führen kann. Das PC-9-Luc-Modell ist hilfreich bei der Bewertung der Entwicklung der T790M-Mutation, möglicher Behandlungen zur Verhinderung der Mutation oder der Behandlung nach der Etablierung der resistenten Zelllinie. Similar to the NCI-H1975-Luc cell line, we have developed the dual implant parameters that allow for the evaluation of both the primary tumor and metastatic brain disease.
In Übereinstimmung mit dem historischen Tumorwachstum für dieses Modell beträgt die Verdopplungszeit des subkutanen Tumorvolumens etwa 4 Tage und erreicht typischerweise die Bewertungsgröße (~1000 mm3) in ungefähr 20 Tagen nach der Implantation (Abbildung 4). Wie erwartet ist das Modell bei intrakranialer Implantation genauso zuverlässig, mit einer per BLI berechneten Verdopplungszeit für das Tumorvolumen von 2,6 Tagen (Abbildung 3 und Bild 2).
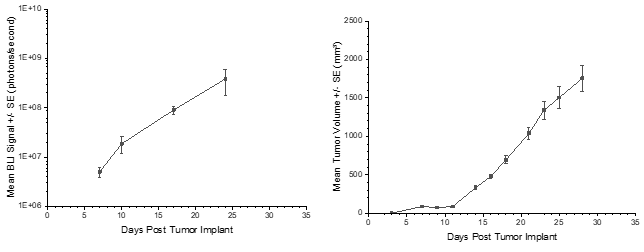
Abbildung 3: PC-9-Luc mittleres BLI-Signal für das Fortschreiten der metastasierenden Erkrankung
Abbildung 4: PC-9-Luc mittleres Wachstum des Primärtumors (SC)

Bild 2: PC-9-Luc repräsentative Bilder des Fortschreitens der metastasierten Gehirnerkrankung
Contact the scientists at Labcorp to request the full cell line list or to learn more about how our subcutaneous, metastatic and orthotopic models, coupled with our optical imaging services, can be applied to your preclinical research.
Verweise
2Cairncross JG, Kim JH, Posner JB. Radiation therapy for brain metastases. Ann Neurol. 1980;7(6):529–541.
Unterhalten wir uns
Kontakt