Autor: Sumithra Urs, PhD | Wissenschaftlerin, Wissenschaftliche Entwicklung
Date: June 2018
In diesem Spotlight präsentieren wir Daten aus unseren ersten Wachstums- und Wirksamkeitsstudien mit dem E0771-Modell. Die hier vorgestellten Daten geben einen Überblick über die Reaktion der E0771-Zelllinie auf immunonkologische Wirkstoffe und Strahlentherapie, um das Design rationaler Kombinationsstudien zu ermöglichen.
Der dreifach negative Brustkrebs (TNBC) ist ein komplexer und aggressiver Subtyp von Brustkrebs ohne Östrogenrezeptor, Progesteronrezeptor und HER2-Amplifikationen, was es schwierig macht, therapeutisch dagegen vorzugehen. Infolgedessen gibt es eine ständige Nachfrage nach besseren Behandlungsmöglichkeiten für TNBC. Um dem Bedarf an TNBC-Modellen gerecht zu werden, haben wir im letzten Monat das EMT6-Modell beleuchtet und nachfolgend stellen wir das E0771-Modell vor, ein weiteres syngenes TNBC-Modell zur Verwendung in der präklinischen Immunonkologie. Die E0771-Zelllinie ist ein sich spontan entwickelndes medulläres Mamma-Adenokarzinom aus C57BL/6-Mäusen.[1] Das elterliche E0771 ist im Vergleich zu 4T1[2] schwach metastatisch und hat homozygote Mutationen im Trp53-und KRAS-Gen.[3]
In diesem Spotlight präsentieren wir Daten aus unseren ersten Wachstums- und Wirksamkeitsstudien mit dem E0771-Modell. Die hier vorgestellten Daten geben einen Überblick über die Reaktion der E0771-Zelllinie auf Immunonkologie-Wirkstoffe und Strahlentherapie, um das Design rationaler Kombinationsstudien zu ermöglichen.
Die Tumorwachstumskinetik für das E0771-Modell ist in Abbildung 1 dargestellt. Die mediane Verdopplungszeit beträgt ~5 bis 6 Tage mit einer stetigen Zunahme des Tumorvolumens ohne offensichtlichen tumorbedingten Körpergewichtsverlust. Diese Wachstumsrate ermöglicht ein dreiwöchiges therapeutisches Fenster zur Beurteilung der Anti-Tumor-Reaktionen. Die Wachstumsparameter von unbehandelten Tumoren und isotypenkontrolliert (Ratte IgG2b) behandelten Tumoren sind ähnlich (Abb. 1).
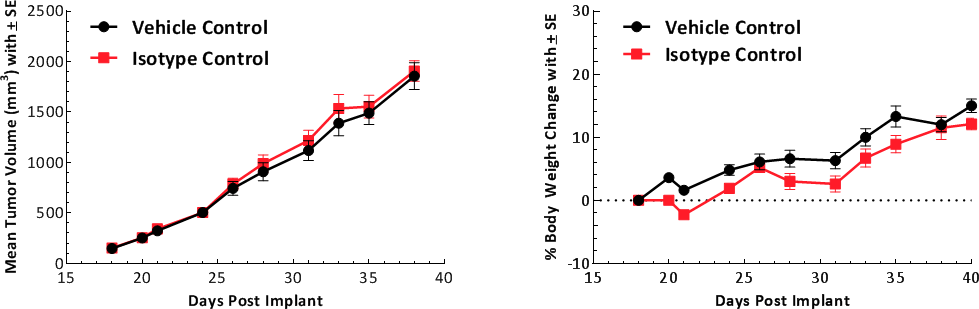
Abb. 1: Wachstumskinetik von subkutanen E0771-Tumoren. Der Graph zeigt Transportmittelkontrolle im Vergleich zur Isotypenkontrolle.
Zusammensetzung tumorinfiltrierender Immunzellen
Die Ausgangszusammensetzung des Tumor-Immunsystems wurde mittels Durchflusszytometrie analysiert und ist in Abb. 2 dargestellt. Das Immunprofil für E0771 wurde aus Tumoren mit einem Volumen von ~750 mm3 erstellt. Die Tumoren haben eine hohe CD45+-Zell-Infiltration (70 %), wobei die T-Zell-Population (CD8+-T-Zellen und CD4+-Helferzellen) gut vertreten ist (jeweils 6 %). Die Treg-Zellpopulation war durchweg niedriger als die CD4+-T-Helferzellen- oder CD8+-T-Zell-Population. Innerhalb der myeloischen Population sind die E0771-Tumoren unter unseren charakterisierten Brustkrebslinien einzigartig, da sie eine Fülle von M-MDSC und ein fast vollständiges Fehlen von G-MDSC aufweisen. M1-Makrophagen waren in den analysierten Tumoren durchweg niedriger als M2-Makrophagen. Diese Zusammensetzung deutet auf eine immunsuppressive Mikroumgebung hin.
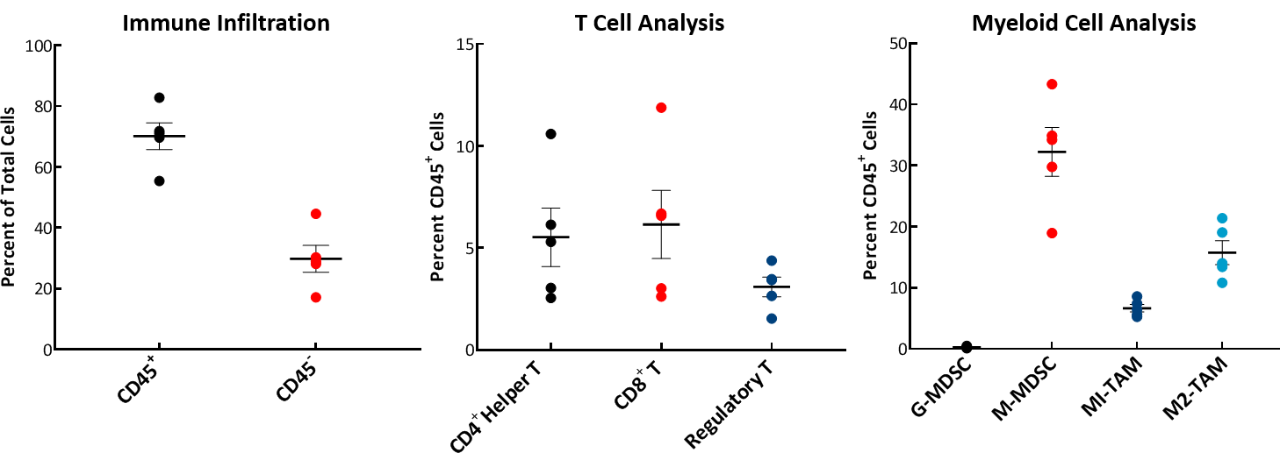
Abb. 2: Tumorimmunprofil von E0771 zeigt Immunzellinfiltration.
Reaktionen auf Behandlungen
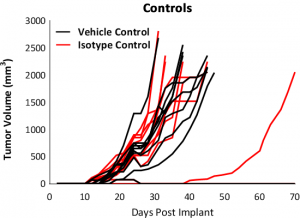
Die Reaktion auf immunmodulatorische Wirkstoffe wurde an Mäusen mit E0771-Tumoren evaluiert, die mit blockierenden Checkpoint-Antikörpern (anti-mPD-1, anti-mPD-L1, anti-mCTLA-4 und anti-mLAG3), kostimulatorischen Antikörpern (anti-mGITR, anti-mOX40 und anti-mCD137) und fokaler Bestrahlung behandelt wurden. Wir testeten die Anti-Tumor-Reaktion auf Checkpoint-Inhibitoren und kostimulatorische Antikörper, bei denen die Dosierung vor der tastbaren Tumorbildung eingeleitet wurde (Abb. 3). Die anti-mPD-1-Behandlung führte zu einer vollständigen Eliminierung des Tumors, während anti-mPD-L1 und anti-mLAG3 mit einer Verzögerung des Tumorwachstums (TGD) von 12,7 und 7,6 Tagen eine signifikante Reaktion zeigten (Abb. 3A). Auch die Behandlung mit den kostimulatorischen Antikörpern anti-mGITR, anti-mCD137 und anti-mOX40 führte zu einem substanziellen Ansprechen mit über 50 % tumorfreien Überlebenden (TFS) und TGD >27 Tagen (Abb. 3B).
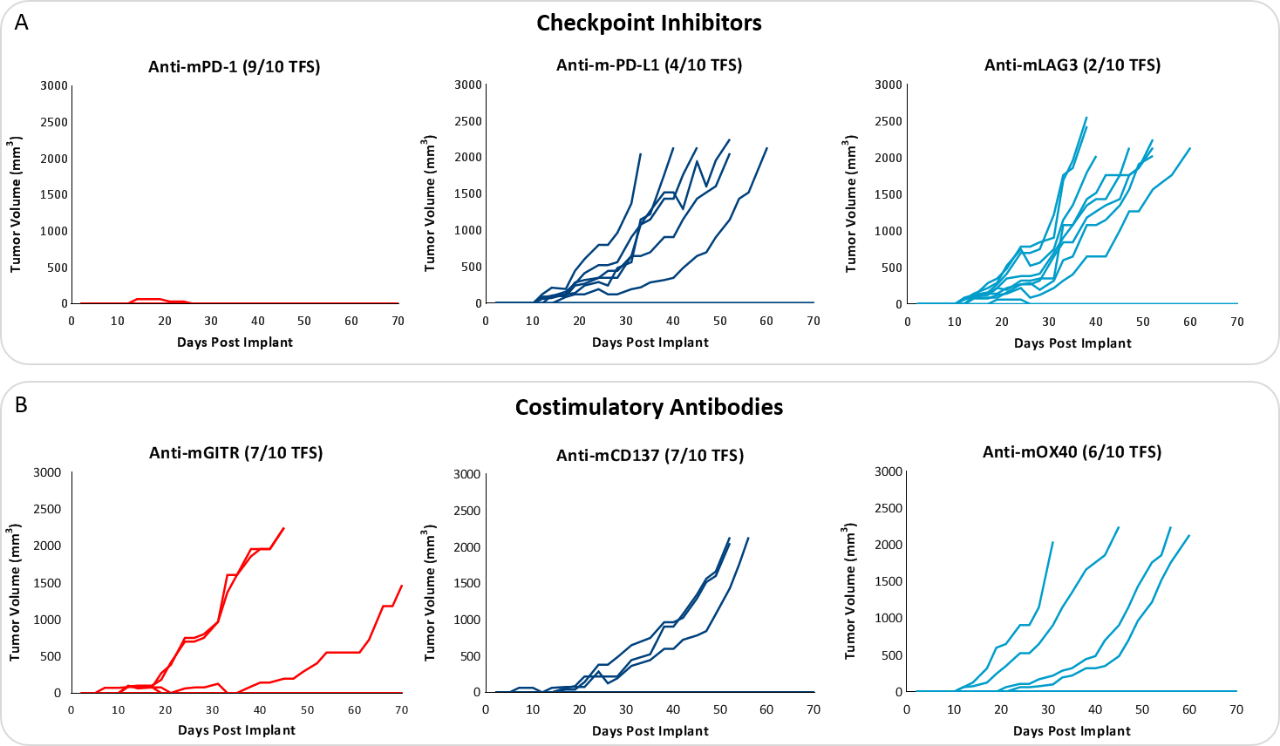
Diese Ergebnisse weisen zwar eindeutig auf die Ansprechbarkeit von E0771 auf eine Immuntherapie hin (Abb. 5), betonen aber gleichzeitig die Bedeutung von Faktoren wie Tumorvolumen zu Behandlungsbeginn und Therapieschema beim Behandlungsergebnis. Die immunsuppressive Mikroumgebung könnte dazu beitragen, das begrenzte Ansprechen bei den meisten der getesteten Immuntherapieschemata zu erklären. Fokale Strahlentherapie kann eine nützliche Behandlungsmethode sein, um eine immunsuppressive Mikroumgebung zu modifizieren. So wurden die fokalen Strahlendosen 5, 10 und 20 Gy getestet und als gut verträglich mit TGD von 5.1, 6 und 10,6 Tagen befunden (Abb. 6). Basierend auf den anfänglich erfassten Strahlendosis-Wirkungsdaten könnte 10 Gy Fokal-Strahlung für Kombinationstherapien empfohlen werden.
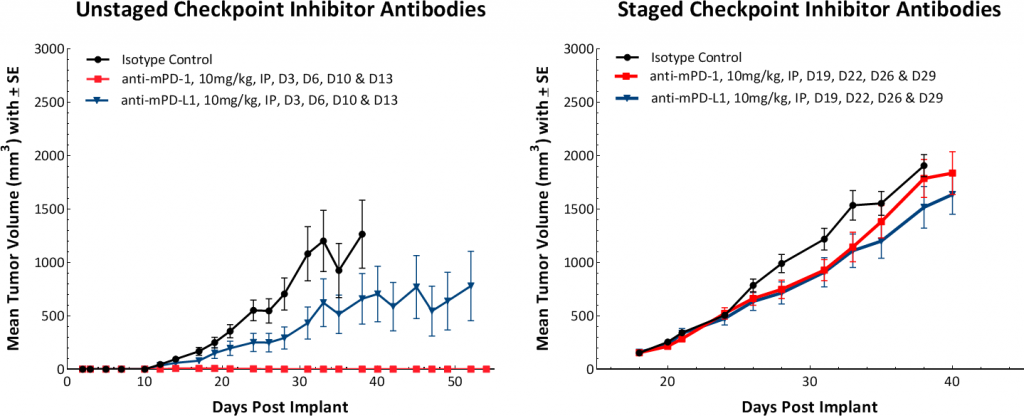
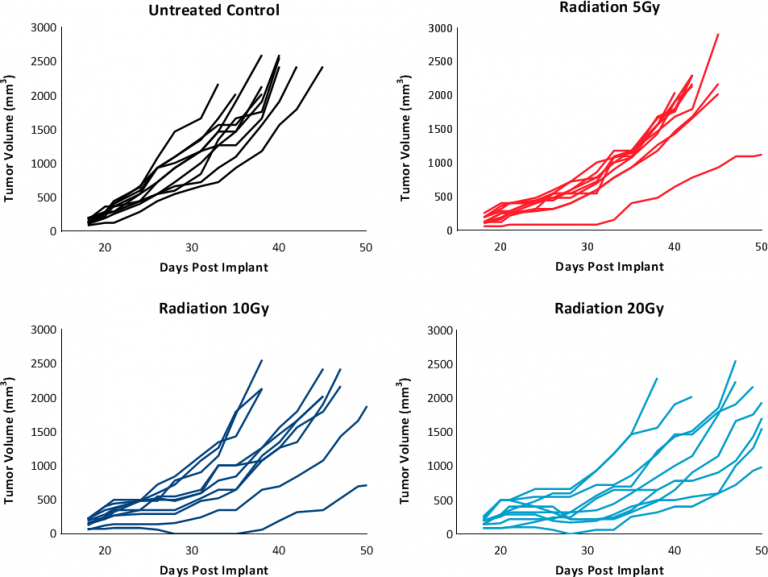
Abb. 6: Ansprechen auf fokale Strahlentherapie.
E0771 – Ein leistungsstarkes präklinisches Immunonkologie-Brustkrebsmodell
TNBC sind im Allgemeinen gegen eine Immun-Monotherapie resistent und gelten aufgrund ihres minimalen Tumor-CD8+-T-Zell-Infiltrats und ihrer geringen Immunogenität aufgrund einer geringen Mutationsbelastung als immunologisch „kalte“ Krebsarten. Angesichts mäßig günstiger Immunzellinfiltration und Reaktion auf die Immuntherapie bietet das E0771-syngene Mammakarzinom-Modell ein bedeutendes Potenzial als präklinisches immunonkologisches Modell. Unsere Daten geben einen Überblick über die Wirkungen der einzelnen Monotherapien und geben Informationen zum Design von Kombinationsstrategien. Behandlungsbeginn und Tumorvolumen spielen eine wesentliche Rolle bei der Bestimmung der Dynamik des Ergebnisses und sollten beim Studiendesign unter Verwendung des E0771-Modells stark berücksichtigt werden.
Please contact us to speak with our scientists about how E0771, or one of our other syngeneic models, can be used for your next immuno-oncology study.
Verweise
[2]Johnston CN, Smith YE, Cao Y et al., (2015). Funktionelle und molekulare Charakterisierung von E0771.LMB-Tumoren, ein neues, von C57BL/6-Mäusen abgeleitetes Modell des spontan metastasierenden Brustkrebses. Dis. Model Mech, Mar; 8(3):237-51.
Unterhalten wir uns
Kontakt