Date: May 2020
Einführung
Die Zelllinie BT-474 blickt auf eine lange Vorgeschichte zurück, doch viele Experten waren der Meinung, dass sie ihren natürlichen Verlauf nehmen und mit der Zeit auslaufen würde.
Angaben der American Type Culture Collection (ATCC) zufolge, wurde die Zelllinie BT-474 1978 von E. Y. Lasfargues ins Leben gerufen nachdem er eine Tumorbiopsie einer 60-jährigen Frau mit fortgeschrittenem, invasivem Duktusbrustkarzinom erhielt. Die Zelllinie wurde später als Östrogen-Rezeptor positiv (ER), Progesteron-Rezeptor positiv (PR) und humaner epidermaler Wachstumsfaktor-Rezeptor 2 positiv eingeordnet (HER2) (1). Diese Daten waren zur Herstellung einer Verbindung des BT-474-Modells, das in der präklinischen Brustkarzinomforschung angewandt wurde, mit tatsächlichen Patienten mit identischem genetischen Profil unentbehrlich.
Der American Association of Cancer Research zufolge, testen ungefähr 80 % aller Brustkrebspatienten ER positiv und -65 % PR positiv. Brustkrebspatienten, die gleichermaßen ER und PR positiv sind, sind mit größerer Wahrscheinlichkeit gute Kandidaten für eine Hormontherapie. Zudem weisen ungefähr 20 % aller Brustkrebsfälle einen Anstieg der HER2-Expression auf, die auf aggressive und schnell wachsende Tumore hindeutet. Die Verbindung zwischen dem präklinischen BT-474-Modell und den Biomarkern der Patienten in Kombination mit dem dringenden Bedarf an zukunftsweisenden Fortschritten in der Brustkarzinombehandlung führten dazu, dass sich dieses Modell in der in-vitro- und der in-vivo-Forschung großer Nachfrage erfreut.
Die BT-474-Herausforderung
Dies wurde jedoch bald widerlegt. Das Problem mit BT-474 (und mehreren weiteren Brustkarzinommodellen) besteht darin, dass sich ihre Anwendung in vivo bekanntermaßen als problematisch erweist.
Bei der subkutanen Implantation oder der Implantation in das Fettgewebe der Brust weiblicher Nacktmäuse verläuft das Wachstum das Tumors extrem langsam (der Tumor verdoppelt sich innerhalb von >20 Tagen) mit großen Unterschieden beim Tumorwachstum und der spontanen Tumorregression. Mehrere Studien belegen dies trotz des Anpassens mehrerer Variablen, wie Mausart (SCID oder nackt), Material des Implantats (Tumorfragmente oder -zellen), Zusatzstoffe der Zellimplantate, (Matrigel® oder Feeder-Layer im Gehirn) und hormonelle Zusatzstoffe (estradiol).
Dies erschwert Wissenschaftlern und Forschern die Anwendung von BT-474, weswegen sie häufig auf andere Modelle mit ähnlichen genetischen Profilen zurückgreifen müssen, die entsprechend einfacher in der Anwendung sind und zuverlässigere Werte liefern.
Da es jedoch nur eine geringe Anzahl von Modellen gibt, die alle Eigenschaften des BT-474 aufweisen (menschliches Brustkarzinom, ER+, PR+ and HER2+), haben wir uns dazu entschieden, an der Optimierung des Modells weiter zu arbeiten. Außerdem ermöglicht uns der Fortschritt und der Zugriff auf NSG-Mäuse, das Wachstum von BT-474 am Stamm mit dem schlechtesten Immunsystem auszuwerten.
Analyse
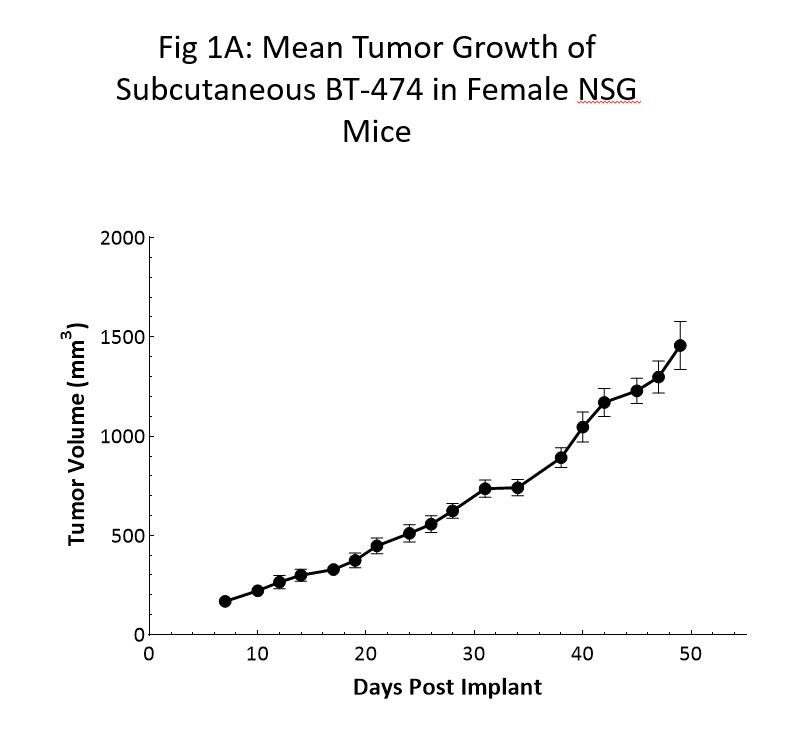
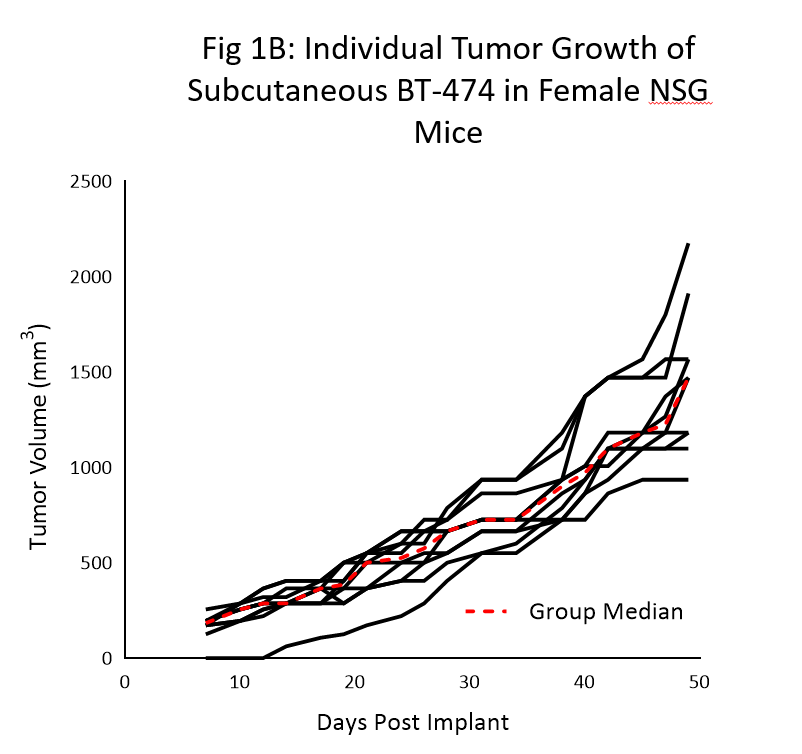
Die Kinetik des Tumorwachstums des BT-474-Modells bei NSG-Mäusen ist in Abbildung 1 dargestellt. Die mediane Verdopplungszeit beläuft sich auf ungefähr 12 Tage, wobei das Volumen des Tumors, bei offenbar ausbleibendem Gewichtsverlust, stetig zunimmt. Die Wachstumsdauer bis zu 150mm3 (etablierte Tumore) belief sich auf 7 Tage nach der Implantation und die Dauer bis zu 1000mm3 (Bewertungsgröße) belieft sich auf 40 Tage nach der Implantation.
Ähnliche Kinetikwerte des Wachstums wurden im Rahmen mehrerer Studien der vergangenen 6 Monate bestätigt.
Die Ergebnisse zeigen deutlich, dass die Verwendung der NSG-Maus bei dem sich jetzt als zuverlässig herausgestellten und vervielfältigbaren Wachstum dieses Modells maßstäblich war.
Ansprechen auf eine auf HER2 ausgelegte Behandlung
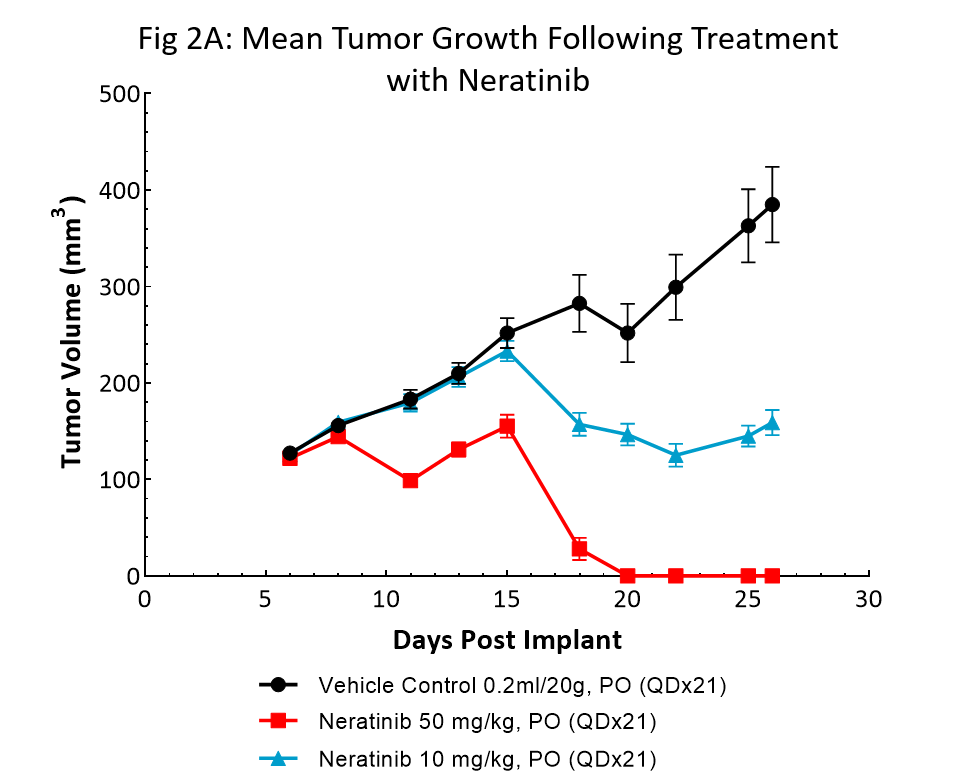
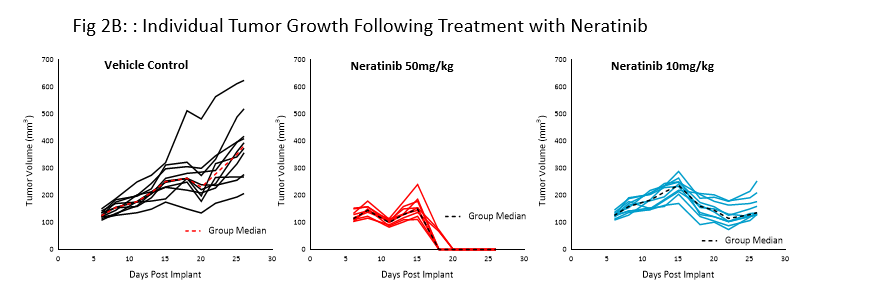
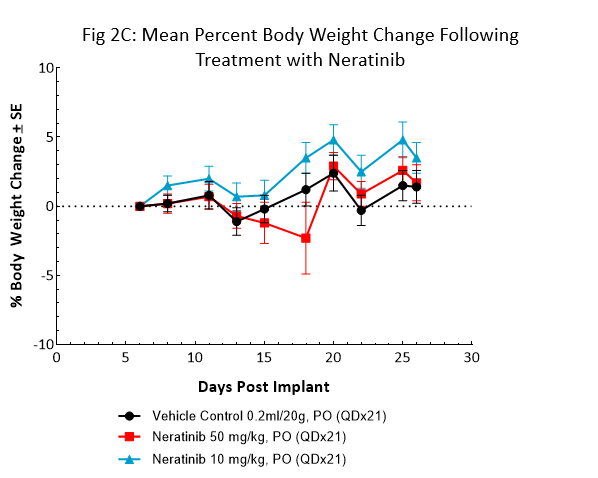
Bei Neratinib (Nerlynx®) handelt es sich um einen von der FDA genehmigten, oral verfügbaren, irreversiblen Tyrosinkinase-Hemmstoff Her2 (humaner epidermaler Wachstumsrezeptor 2) und EGFR (EGF-Rezeptor). Die Auswertung des Ansprechens von NSG-Mäusen mit subkutanen BT-474-Tumoren auf die tägliche Behandlung mit neratinib mit der Dosierung von 10 und 50 mg/kg an 21 aufeinander folgenden Tage finden Sie in Abb. 2.
Die Behandlung mit neratinib mit beiden Dosierungen wurde in Verbindung mit minimalen Veränderungen des Körpergewichts gut vertragen. Die Verabreichung von 50mg/kg resultierte in einer vollständigen Tumorregression bei allen Mäusen. Die Behandlung mit der niedrigeren Dosierung bewirkte die Hemmung von 50 % des Tumorwachstums, was auf das Ansprechen auf die Dosierung hindeutet. Diese Werte sind deutliche Belege dafür, dass das BT-474-Modell HER2 seine Überexpression und Abhängigkeit beibehielt.
BT-474 - Ein neuer Ansatz für ein effektives, präklinisches Mittel
Angesichts des anhaltenden Bedarfs an neuen gezielten Brustkarzinombehandlungen, von kleinen Molekülen und Antikörpern bis hin zu zellbasierten Therapien, liegt es in unserer Verantwortung, die einzigartigen Zelllinien, die uns für die Forschung in der Wirkstoffentwicklung zur Verfügung stehen, zu optimieren.
Die Anwendung von Modellen wie BT-474, welche die Lücke zwischen dem präklinischen Modell und dem Krebspatienten schließen können, nehmen eine essenzielle Stellung ein. Die Optimierung unseres BT-474 Brustkarzinommodells bei NSG-Mäusen ist eine bedeutende Weiterentwicklung unseres validierten Brusttumormodells, und wir arbeiten weiterhin an der Bewertung weiterer spezifischer HER2-Therapien, wie Herceptin, des BT-474 Modells.
Please contact us to speak with our scientists about how BT-474 or one of our other models can be used for your next oncology study.
Verweise
Unterhalten wir uns
Kontakt