Author: Dylan Daniel, PhD, Director, Scientific Development
Date: December 2016
Brustkrebs ist nach Lungenkrebs die zweithäufigste Malignität bei Frauen in den USA, wobei im Jahr 2016 mit geschätzten 246.000 Neuerkrankungen und 40.450 erwarteten Todesfällen gerechnet wird. Es gibt viele Behandlungsmöglichkeiten für Brustkrebs, einschließlich Operation, Strahlentherapie, Antiöstrogentherapie, gezielte Therapien (z. B. Trastuzumab) und Chemotherapie. Trotz dieser therapeutischen Fortschritte bleibt die metastatische Erkrankung eine bedeutende Todesursache. Die Immuntherapie hat in den letzten fünf Jahren bemerkenswerte Fortschritte erzielt, da vier T-Zell-Immun-Checkpoint-Inhibitoren zugelassen wurden. Während keiner dieser Checkpoint-Inhibitoren bei Brustkrebs zugelassen ist, laufen derzeit über 60 klinische Studien zu Brustkrebs mit Checkpoint-Inhibitoren gegen P-1 oder PD-L1 und über 20 klinische Studien mit CTLA-4-Inhibitoren.
Da Checkpoint-Inhibitoren und andere Klassen von Immuntherapien ein intaktes Immunsystem erfordern, um Aktivität hervorzurufen, sind syngene Mausmodelle von Brustkrebs eine wichtige Option für die präklinische Prüfung neuer Wirkstoffe. Labcorp has fully characterized the 4T1-luc2 mammary carcinoma model derived from Balb/c mice as an orthotopic model to support studies with novel immuno-oncology agents. Orthotope 4T1-luc2-Tumoren metastasieren zu Lymphknoten und zur Lunge, was es zu einem wertvollen Modell macht, um die Wirkung von Therapien sowohl auf den Primärtumor als auch auf metastatische Erkrankungen mithilfe von Biolumineszenz-Bildgebung zu untersuchen. Das Wachstum von 4T1-luc2-Tumoren ist bei immundefizienten Stämmen und immunkompetenten Balb/c-Mäusen äquivalent, was darauf hindeutet, dass 4T1-luc2 ein schwach immunogener Tumor ist (Abbildung 1).
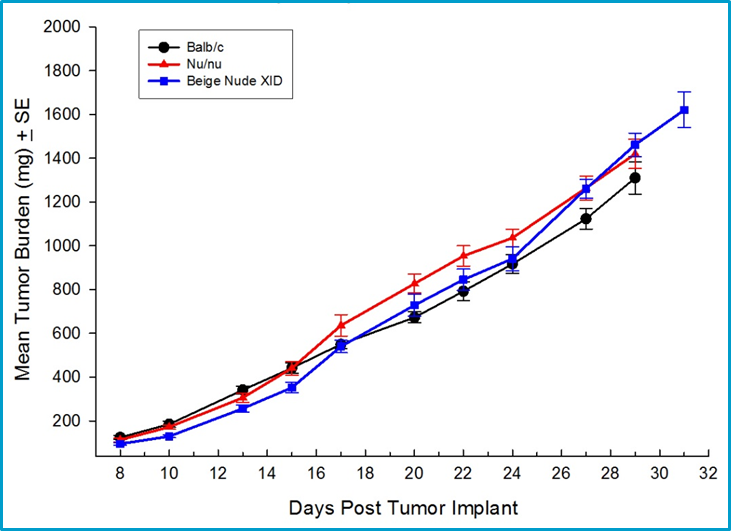
Fig. 1: Orthotopes Wachstum von 4T1-luc2 in mehreren Mäusestämmen, einschließlich syngener Balb/c-Mäuse.
Wirksamkeitsstudien mit Antikörpern gegen PD-1 oder PD-L1 werden durch eine tödliche Überempfindlichkeitsreaktion bei Mäusen mit 4T1-Tumoren behindert.1 Es ist möglich, zwei Dosen ohne Toxizität zu verabreichen, eine fortlaufende Dosierung ist jedoch nicht möglich. Stattdessen wurde die Wirksamkeit von Anti-CTLA-4 in Kombination mit lokalisierter Strahlung bewertet. Ein Hamster-Anti-CTLA-4-Antikörper wurde verwendet, und unerwarteterweise zeigte die Hamster-Isotypkontrolle bei einigen Mäusen eine signifikante Aktivität (Abbildung 2A), die sich nicht von der Anti-CTLA-4-Aktivität unterschied (Abbildung 2B). Mit lokalisierter Bestrahlung war ein therapeutischer Nutzen verbunden (Abbildung 2C), aber keine deutliche Verbesserung bei der Kombination von Bestrahlung und Anti-CTLA-4 (Abbildung 2D).
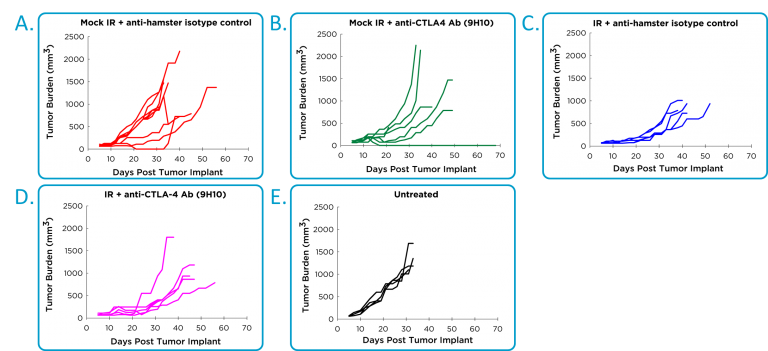
Abb. 2: Wirksamkeit von Anti-CTLA-4 und lokalisierter Strahlentherapie im orthotopen 4T1-luc2Brusttumor-Modell.
Die metastatische Belastung wurde unter Verwendung der Biolumineszenz-Bildgebung bewertet. Es werden repräsentative Bilder des Fortschreitens der Metastasen in unbehandelten Mäusen gezeigt (Abbildung 3A). Die mit Anti-CTLA-4 behandelten Mäuse hatten im Vergleich zu den Mäusen, die mit der Isotypkontrolle behandelt wurden, eine verringerte metastatische Tumorlast (Abbildung 3B). Lokalisierte Strahlung führte auch zu einer signifikanten Verringerung der metastatischen Belastung, es scheint jedoch keine Verbesserung über die Einzelwirkstoffaktivität von Anti-CTLA-4 hinaus in der Kombinationsgruppe zu geben.
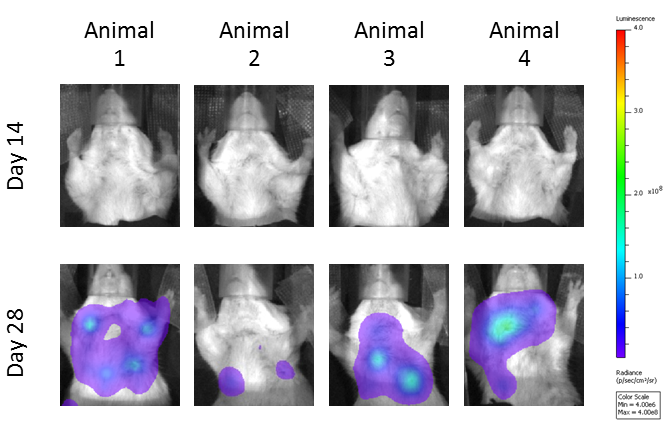
Abb. 3: Bewertung der gesamten metastasierten Tumorlast im Laufe der Zeit durch Biolumineszenz-Bildgebung:
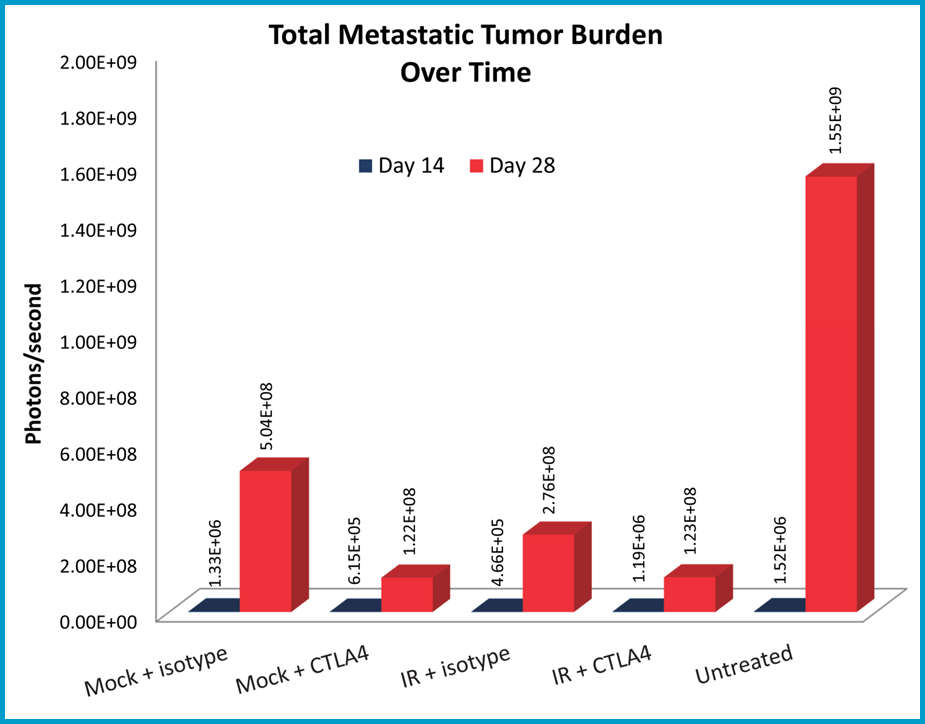
Abb 3B: Quantifizierung der metastatischen Belastung und des Ansprechens auf die Behandlung.
Die Strahlung in dieser Studie wurde unter Verwendung von Bleiabschirmung lokalisiert, um die Gesamtkörperstrahlung zu reduzieren. Einige Tiere zeigten jedoch immer noch Anzeichen von Strahlungstoxizität. Labcorp now offers focal beam radiation capabilities using the small animal radiation research platform (SARRP) by Xstrahl which reduces systemic radiation toxicity.
![Abb. 4: Wirksamkeit der Anti-CTLA-4-Therapie mit Maus-Isotyp-Anti-CTLA-{[# 2]}-Antikörper.](https://biopharma.labcorp.com/industry-solutions/by-therapeutic-area/oncology/preclinical/tumor-spotlights/4t1-luc2-an-orthotopic-mammary-cancer-model-to-support-novel-immuno-oncology-drug-discovery/_jcr_content/root/responsivegrid_left/image_copy_copy_copy_2142731733.coreimg.png/1670865515675/1578319795510.png)
Abb. 4: Wirksamkeit der Anti-CTLA-4-Therapie mit Maus-Isotyp-Anti-CTLA-{[# 2]}-Antikörper.
Die unspezifische Antitumoraktivität, die mit der Verwendung eines Hamsterantikörpers in dem 4T1-luc2-Modell verbunden ist, führte zu einer nachfolgenden Studie unter Verwendung eines Maus-Anti-CTLA-4-Antikörpers. Maus-Anti-CTLA-4-Behandlung führte zu minimaler Aktivität im 4T1-luc2-Modell (Abbildung 4), bietet aber einen potenziellen Kombinationspartner für vom Kunden gesponserte Studien mit neuartigen immunonkologischen Wirkstoffen. Darüber hinaus haben wir eine umfassende Durchflusszytometrie-Immunprofilierung von 4T1-luc2-Tumoren einschließlich der Quantifizierung von CD4-T-Zellen, CD8-T-Zellen, regulatorischen T-Zellen, granulozytischen MDSC, monozytische MDSC, M1- and M2-Tumor-assoziierte Makrophagen (TAM) (Abbildung 5). Das Modell ist gut charakterisiert und für vom Kunden gesponserte Studien mit neuartigen Immuntherapien oder Wirkstoffen verfügbar, die sich gut mit kommerziell erhältlichen Immuntherapien kombinieren lassen. Please contact us for further information and find out how Labcorp can help with your next study.
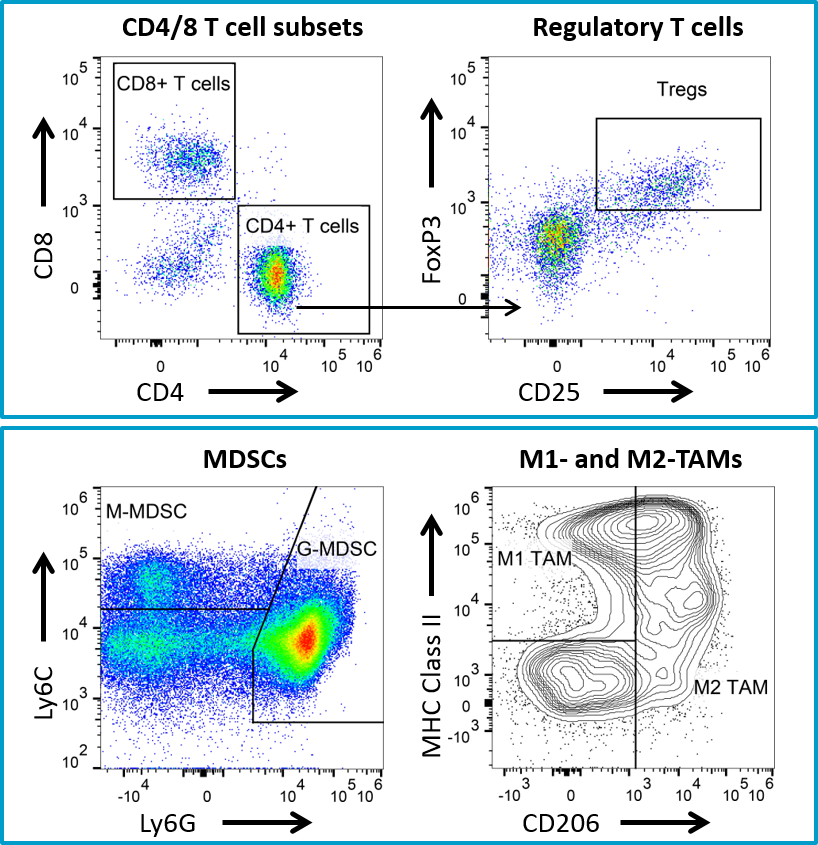
Fig. 5: Durchflusszytometrie-Immunprofilierung für 4T1-luc2-Tumoren
1Mall et al., OncoImmunology (2016), Vol. 5 (2): e1075114
Hinweis: Die Studien wurden in Übereinstimmung mit den geltenden Tierschutzbestimmungen in einer von der AAALAC akkreditierten Einrichtung durchgeführt.
Verweise
Unterhalten wir uns
Kontakt